

Vol. 38 (Nº 23) Año 2017. Pág. 8
Mara Luana ENGEL 1; Antonio Rioyei HIGA; Giovana Bomfim de ALCANTARA; Paulo Cesar FLÔRES JUNIOR; Izabele Domingues SOARES
Recibido: 24/11/16 • Aprobado: 15/12/2016
RESUMO: Devido ao grande interesse comercial para a fabricação do tanino e cavacos, busca-se otimizar técnicas de propagação clonal de Acacia mearsii almejando sua silvicultura clonal em larga escala. Assim, o objetivo do trabalho foi verificar a influência de diferentes formas de aplicação e concentrações de ácido indol butírico (AIB) no enraizamento de miniestacas de três diferentes clones. Testou-se 7 concentrações de AIB (0, 1000, 2000, 3000, 4000, 5000 e 6000m g L-1) na forma líquida e na forma de pó, com fatorial 2x7 em blocos casualizados, com 4 repetições e 6 miniestacas por parcela, para os diferentes clones. As variáveis avaliadas foram: porcentagem de miniestacas vivas enraizadas, número de raízes por miniestaca e comprimento médio de raízes por miniestaca. Existe predisposição da espécie para o enraizamento e os resultados variaram em função da concentração de AIB. Porém a resposta foi diferente conforme o material genético, sendo o clone B com maior porcentagem de enraizamento (85%). |
ABSTRACT: Due to the great commercial interest for the manufacture of tannin and chips, seeks to optimize techniques of clonal propagation of Acacia mearsii aiming your clonal forestry on a large scale. The objective of the study was to investigate the influence of different forms of application and indole butyric acid (IBA) concentrations on rooting cuttings of three different clones. Was tested 7 IBA concentrations (0, 1000, 2000, 3000, 4000, 5000 and 6000mg L-1) in liquid form and as powder, a factorial 2x7 randomized blocks, with 4 replications 6 minicuttings per share, for the different clones. The variables evaluated were: percentage of rooted cuttings alive, root number per minicutting and average length of roots minicutting. There is predisposition of the species for rooting and results varied as a function of IBA concentration. However, the response was different according to the genetic material, with clone B having the highest percentage of rooting (85%). |
Diante do crescente interesse pelo uso de clones nos projetos florestais, tem-se percebido um grande avanço tecnológico nos processos de seleção e clonagem de material superior. Segundo Alfenas et al. (2004), a utilização da propagação vegetativa de espécies florestais, associada a programas de melhoramento, tem como finalidade acelerar o crescimento e gerar madeira de qualidade e homogênea. Em outras espécies florestais, além dos gêneros Eucalyptus e Pinus, a silvicultura clonal está em nível de desenvolvimento no Brasil, com diferentes graus de avanço (Xavier et al., 2013), e entre essas espécies está o gênero das Acácias, dentre elas, Acacia mearnsii De Wild., também conhecida como acácia-negra.
O cultivo de acácia-negra no Brasil, é exclusivamente encontrada no Rio Grande do Sul, com os primeiros plantios comerciais iniciando na década de 1930. Um aspecto vantajoso nas plantações de acácia-negra é sua característica multifuncional, atrelada aos serviços ambientas e também utilização em sistemas agroflorestais.
A matéria prima mais importante comercialmente da A. mearnsii é o tanino, pois é uma das melhores espécies em termos de rendimento por árvore e de qualidade da matéria-prima. O tanino é utilizado na produção de tintas, também para produção de inibidores de corrosão, promotores de fluxo de líquidos em tubos, produtos farmacêuticos (Seiger, 2002), adesivos para chapas de madeira e floculantes para tratamento de água, além de outros produtos como dispersantes, resinas, quelantes e conservantes (Simon, 2005).
Para a acácia negra, a propagação vegetativa é uma alternativa para a obtenção de indivíduos com características genéticas superiores (Eldridge et al., 1994). Porém a falta de técnicas adequadas para tal prática tem limitado a utilização de vários métodos de propagação vegetativa em larga escala para a espécie. Dentre essas várias técnicas de propagação vegetativa destacam-se a estaquia e a miniestaquia que visam atender os objetivos da silvicultura clonal. A propagação vegetativa é usada em programas de melhoramento genético e de conservação da espécie, em razão do aumento da uniformidade do crescimento, qualidade e quantidade de madeira a ser produzida (Valeri et al., 2012). Porém esta técnica ainda apresenta limitações nas taxas de enraizamento adventício do material clonal de genótipos superiores.
É comum que algumas espécies apresentam limitações na obtenção de mudas por propagação vegetativa, essas espécies, quando classificadas como relativamente fáceis de enraizar, ao serem submetidas a tratamentos com auxinas sintéticas respondem bem à emissão radicial (Hartmann et al., 2011). O conhecimento das melhores técnicas de propagação vegetativa, aliadas às substâncias que promovem aumento no enraizamento, contribuem para melhorar a utilização de espécies com ganhos de produtividade (Xavier et al., 2011). As auxinas são uma classe de reguladores vegetais envolvidos em muitos aspectos do crescimento e desenvolvimento de plantas. Quando aplicada em órgãos isolados, a auxina, dependendo de sua concentração, pode aumentar a resposta rizogênica (Goulart et al., 2008). Nesse contexto, o ácido indol butírico tem se revelado como um dos reguladores exógenos mais eficientes na indução de primórdios radiciais (Camargo e Vieira, 2001).
Portanto, visando otimizar as técnicas de propagação vegetativa de acácia negra, o objetivo do trabalho foi verificar o efeito de diferentes formas de aplicação e diferentes concentrações de AIB no enraizamento de miniestacas de clones de interesse comercial de Acacia mearnsii.
O experimento foi conduzido no município de Montenegro, RS, localizado a 29º41'19" de latitude sul e 51º27'40" de longitude oeste, a uma altitude de 31 metros (IBGE, 2010). As avaliações foram realizadas no viveiro pertencente à empresa TANAGRO S.A. O viveiro está localizado na Zona Subtropical Sul, com média anual de temperatura de 19°C, normais pluviométricas anuais superiores a 1800mm e umidade relativa do ar superior a 70% (Ferraro e Hasenack, 2000).
A coleta de miniestacas para os testes de enraizamento foi realizada nos minijardins clonais á céu aberto da empresa. Foram realizados experimentos testando-se diferentes tratamentos com aplicação de AIB e estes foram instalados na estação de verão, mais precisamente no mês de janeiro, época de maior produção e potencial de enraizamento.
Os minijardins clonais são formados por canaletões de 1,10 a 1,20m, contendo material inerte (areia) em sistema semi-hidropônico. São compostos de minicepas, com espaçamento de 10x15cm, obtidas pelo enraizamento de miniestacas dos respectivos clones do estudo, que tiveram seus ápices podados constituindo, assim, as minicepas que forneceram as brotações (miniestacas) para a realização do experimento.
A irrigação e a nutrição mineral foram efetuadas através do sistema automatizado de fertirrigação por inundação, de maneira que somente o sistema radicular permanecia em contato com a solução nutritiva. A periodicidade da fertirrigação variou em função do clima. Os adubos utilizados foram: Nitrato de Potássio a 0,3g L-1; Monopotássio de Fosfato a 0,1g L-1; Nitrato de Magnésio a 0,24g L-1; Nitrato de Cálcio a 0,85g L-1 e Quelato de Fe (6% Fe) a 50mg L-1. Para os micronutrientes era realizada uma solução de: Molibdato de Sódio a 0,5g L-1; Ácido Bórico a 15g L-1; Sulfato de Cobre a 0,5g L-1; Sulfato de Manganês a 20g L-1 e Sulfato de Zinco a 10g L-1.
As miniestacas foram coletadas do minijardim clonal e acondicionadas em caixas térmicas. Para manter as condições de turgescência do material vegetativo pulverizou-se água, em intervalos de 10 minutos, até a confecção das miniestacas, com dimensões variando de 10 a 12 cm de comprimento e com um a dois pares de folhas, tendo a área foliar reduzida à metade.
Foram avaliados três diferentes clones, denominados A, B e C. Foram testadas duas vias de aplicação de AIB (Ácido Indol Butírico), via pó e via líquida, em sete diferentes concentrações: 0, 1000, 2000, 3000, 4000, 5000, 6000 mg L-1. Compondo assim, um fatorial 2x7, em delineamento em blocos casualizados, com 4 repetições e 6 plantas por parcela, totalizando 336 miniestacas.
As miniestacas foram colocadas em bandejas com tubetes de 55cm³, utilizando substrato composto por 50% de casca de arroz carbonizada e 50% de vermiculita média, com aplicação de 3kg/m³ de osmocote. As miniestacas permaneceram em casa de vegetação com temperatura média em torno de 25 a 30°C, umidade relativa do ar de 90 a 95%. A frequência de nebulização foi de 10 segundos a cada 15 minutos das 7:00 às 18:00, com esta frequência variando conforme a temperatura do dia.
As avaliações das miniestacas foram realizadas aos 45 dias e as características avaliadas foram: porcentagem de enraizamento, número de raízes por miniestaca e comprimento médio das 3 maiores raízes formadas por miniestaca.
Inicialmente as variâncias dos tratamentos foram avaliadas quanto à sua homogeneidade pelo teste de Bartlett. As variáveis cujas variâncias mostraram-se homogêneas tiveram as médias dos tratamentos testadas por meio do teste de F. Posteriormente foi realizada a análise de regressão para o fator quantitativo altura. As médias dos tratamentos foram comparadas pelo teste de Scott – Knott e as análises estatísticas foram realizadas com o software Assistat 7.7.
Com base nos dados amostrados o resultado da análise de variância (Tabelas 1, 2 e 3) mostrou que não houve interação entre os fatores forma de aplicação e concentração de AIB, em nenhuma das variáveis, para o clone A. Houve efeito significativo para o fator concentração de AIB apenas para a característica número de raízes por miniestaca (NR) (p>0,01) (Tabela 1). A interação entre forma de aplicação e concentração de AIB também não foi significativa para o clone B, em nenhuma das variáveis. Para este clone, o efeito significativo foi observado para o fator aplicação de AIB quanto a característica comprimento médio de raízes por miniestaca (CMR) (p>0,01), bem como para NR (p>0,05). Já o fator concentração foi significativo (p>0,01) apenas para NR, como pode ser observado na Tabela 2.
Para o clone C (Tabela 3) houve interação entre os fatores (p>0,05) apenas para CMR, ou seja, as miniestacas responderam de maneira diferenciada quanto a CMR em função da aplicação e da concentração de IBA. Para este mesmo clone, também houve significância para os fatores de forma isolada, sendo a forma de aplicação significativa (p>0,01) para a característica CMR, e a concentração de AIB significativa para porcentagem de miniestacas enraizadas (E%) (p>0,05) e CMR (p>0,01).
TABELA 1 - ANÁLISE DE VARIÂNCIA DO CLONE A, PARA PORCENTAGEM DE ENRAIZAMENTO, NÚMERO DE RAÍZES POR MINIESTACA E COMPRIMENTO MÉDIO DE RAÍZES POR MINIESTACA PARA A. mearnsii DE WILDEMAN, TRATADAS COM DIFERENTES CONCENTRAÇÕES DE AIB SOB DIFERENTES FORMAS DE APLICAÇÃO, NO MÊS DE JANEIRO DE 2016.
Fontes de Variação |
GL |
Quadrado Médio |
||
E% |
NR |
CMR (cm) |
||
Tratamentos |
13 |
412,47ns |
71,33** |
4,55ns |
Aplicação AIB |
1 |
44,64ns |
9,269ns |
1,58ns |
Concentração AIB |
6 |
355,49ns |
148,65** |
5,81ns |
Aplicação x Concentração AIB |
6 |
530,75ns |
4,35ns |
3,78ns |
Blocos |
3 |
5415,01** |
91,58** |
82,72** |
Resíduo |
39 |
575,27 |
10,40 |
5,18 |
Total |
55 |
|||
Teste de Bartlett (X2) |
10,42* |
20,19* |
19,99* |
|
Coeficiente de Variação (%) |
39,31 |
38,59 |
26,40 |
|
**Significativo ao nível de 1% de probabilidade; *Significativo ao nível de 5% de probabilidade; ns não significativo; 1 Variável cujo teste de homogeneidade de variâncias não se aplica. Sendo: GL = graus de liberdade; E(%) = porcentagem de miniestacas enraizadas; NR = número de raízes por miniestaca e CMR = comprimento médio das três maiores raízes por miniestaca.
TABELA 2 - ANÁLISE DE VARIÂNCIA DO CLONE B, PARA PORCENTAGEM DE ENRAIZAMENTO, NÚMERO DE RAÍZES POR MINIESTACA E COMPRIMENTO MÉDIO DE RAÍZES POR MINIESTACA PARA A. mearnsii DE WILDEMAN, TRATADAS COM DIFERENTES CONCENTRAÇÕES DE AIB SOB DIFERENTES FORMAS DE APLICAÇÃO, NO MÊS DE JANEIRO DE 2016.
|
|
Quadrado Médio |
|||
Fontes de Variação |
GL |
E% |
NR |
CMR (cm) |
|
Tratamentos |
13 |
296,09ns |
68,76** |
1,26ns |
|
Aplicação AIB |
1 |
178,57ns |
33,25* |
7,08** |
|
Concentração AIB |
6 |
433,20ns |
135,98** |
0,26ns |
|
Aplicação x Concentração AIB |
6 |
178,57ns |
7,45ns |
1,28ns |
|
Blocos |
3 |
218,25ns |
59,96** |
2,30ns |
|
Resíduo |
39 |
250,30 |
4,74 |
0,88 |
|
Total |
55 |
|
|
|
|
Teste de Bartlett (X²) |
19,97* |
25,05** |
29,70** |
||
Coeficiente de Variação (%) |
|
18,59 |
22,90 |
9,23 |
|
**Significativo ao nível de 1% de probabilidade; *Significativo ao nível de 5% de probabilidade; ns não significativo; 1 Variável cujo teste de homogeneidade de variâncias não se aplica. Sendo: GL = graus de liberdade; E(%) = porcentagem de miniestacas enraizadas; NR = número de raízes por miniestaca e CMR = comprimento médio das três maiores raízes por miniestaca.
TABELA 3 - ANÁLISE DE VARIÂNCIA DO CLONE C, PARA PORCENTAGEM DE ENRAIZAMENTO, NÚMERO DE RAÍZES POR MINIESTACA E COMPRIMENTO MÉDIO DE RAÍZES POR MINIESTACA PARA A. mearnsii DE WILDEMAN, TRATADAS COM DIFERENTES CONCENTRAÇÕES DE AIB SOB DIFERENTES FORMAS DE APLICAÇÃO, NO MÊS DE JANEIRO DE 2016.
Fontes de Variação |
GL |
Quadrado Médio |
||
E% |
NR |
CMR (cm) |
||
Tratamentos |
13 |
1321,73* |
11,79ns |
14,16** |
Aplicação AIB |
1 |
496,03ns |
0,08ns |
51,70** |
Concentração AIB |
6 |
1903,11* |
19,59ns |
11,90** |
Aplicação x Concentração AIB |
6 |
877,98ns |
5,94ns |
10,18* |
Blocos |
3 |
191,80ns |
17,44ns |
4,38ns |
Resíduo |
39 |
665,44 |
13,92 |
3,49 |
Total |
55 |
|
|
|
Teste de Bartlett (X²) |
8,47* |
15,77* |
32,00** |
|
Coeficiente de Variação (%) |
|
42,91 |
65,52 |
21,02 |
**Significativo ao nível de 1% de probabilidade; *Significativo ao nível de 5% de probabilidade; ns não significativo; 1 Variável cujo teste de homogeneidade de variâncias não se aplica. Sendo: GL = graus de liberdade; E(%) = porcentagem de miniestacas enraizadas; NR = número de raízes por miniestaca e CMR = comprimento médio das três maiores raízes por miniestaca.
Para a porcentagem de miniestacas enraizadas, apesar de não haver significância para ambos os fatores, a média de enraizamento foi de 61,01%, 85,12% e 60,12% (Tabela 4) para os clones A, B e C, respectivamente, mostrando que a espécie possui potencialidade para a propagação vegetativa por miniestaquia independente do tratamento utilizado, e isso sugere que estas respostas morfogenéticas são fortemente influenciadas pela juvenilidade do material. Lattuada et al. (2012), em estudos com propagação vegetativa em pintagueira observou que a juvenilidade da planta matriz contribui positivamente para as taxas de enraizamento da espécie (69,07%).
Para espécies florestais consideradas de mais fácil enraizamento, como do gênero Eucalyptus, em estudos de aplicação de AIB para clones de E. grandis (Wendling e Xavier, 2005), os autores também não observaram grande efeito da concentração do regulador no enraizamento, atingindo taxas de até 76,3% de enraizamento. Para esta mesma espécie, Titon et al. (2003) obtiveram taxas de enraizamento entre 90 e 100% para diferentes clones, com a aplicação de 1000mg L-1. Já para outras espécies de Eucalyptus com aplicação de AIB, obtem-se taxas de 58,3 a 100% de enraizamento para clones híbridos de E. globulus (Borges et al., 2011); 4,62% a 56,20% de enraizamento para clones híbridos de E. benthamii x E. dunnii, em diferentes sazonalidades (Brondani et al., 2010); médias de 80% de enraizamento para diferentes clones de E. cloenziana (Almeida et al., 2007).
Para outras espécies florestais da mesma família da acácia negra os resultados são variáveis. Para miniestacas de Anadenathera macrocarpa tratadas com AIB variando de 0 a 6000mg L-1, Dias et al. (2012) encontraram resultados de 80 a 98% de enraizamento com baixa influência do regulador vegetal; para miniestacas de Erythrina falcata com diferentes concentrações de AIB, foram encontrados resultados que variam de 0 a 85,5% de enraizamento em diferentes estudos por Cunha et al. (2008) e Rêgo et al. (2003); miniestacas de Acacia baileyana atingiram até 36% de enraizamaneto com a aplicação de 5000mg L-1 de AIB em estudos de Schwarz et al. (2016).
Apesar de haver pouca variação no resultado de enraizamento entre as concentrações de AIB, pode-se notar que em valores numéricos, maiores porcentagens de enraizamento foram encontradas nas concentrações de 6000mg L-1 (70,83% e 79,17%, para os clones A e C), comparadas com o tratamento onde não se aplicou o regulador vegetal (54,17% e 41,67%) e para o clone B, com maiores porcentagens, a concentração de 4000 mg L-1, mostrou-se promissora, com a maior taxa de enraizamento (93,75%) (Tabela 4). Esses valores indicam que a aplicação do regulador vegetal AIB tem certa influência na porcentagem de enraizamento de miniestacas de acácia negra, complementarmente ao material genético.
Resultados de enraizamento abaixo desses valores são encontrados para alguns clones do gênero Eucalyptus. Estudos comprovam que para diferentes clones de E. benthamii x E. dunnii a faixa situada entre os tratamentos de 4000 e 6000mg L-1 de AIB induz os melhores resultados de enraizamento que promove uma máxima de 41,97% de miniestacas enraizadas (Brondani et al., 2010). De acordo com Hartmann et al. (2011), quando se faz a aplicação de reguladores vegetais, há efeito de estímulo à indução radicial, porém, esse estímulo vai até um ponto máximo, a partir do qual se torna inibitório. No presente trabalho não foi possível verificar este limite, no qual seria possível observar redução nos índices de enraizamento deste material, uma vez que maiores resultados foram encontrados nas maiores concentrações de AIB aplicadas.
A forma de aplicação em pó ou em líquido não apresentou nenhuma influência no desempenho para o enraizamento, com valores variando entre 57,14% a 86,90% (Tabela 4). Semelhante aos resultados deste estudo, o trabalho de Almeida et al., (2007), mostra que a forma de aplicação do AIB também não interferiu nos índices de enraizamento de clones de E. cloeziana, apenas interferiu no vigor fisiológico da muda posterior ao enraizamento, sendo a forma de pó mais vantajosa. Por isso é importante observar as vantagens e desvantagens de cada forma de aplicação.
TABELA 4- PORCENTAGEM DE MINIESTACAS ENRAIZADAS DE A. mearnsii DE WILDEMAN APÓS 45 DIAS DE ESTAQUEAMENTO, EM FUNÇÃO DE DIFERENTES CONCENTRAÇÕES DE AIB E DIFERENTES FORMAS DE APLICAÇÃO PARA TRÊS DIFERENTES CLONES A, B E C.
Aplicação de AIB |
Porcentagem de Miniestacas Enraizadas (E%) |
|||||||
0 mg L-¹ |
1000 mg L-¹ |
2000 mg L-¹ |
3000 mg L-¹ |
4000 mg L-¹ |
5000 mg L-¹ |
6000 mg L-¹ |
Médias |
|
CLONE A |
||||||||
Pó |
58,33 |
58,33 |
58,33 |
50,00 |
66,67 |
70,83 |
58,33 |
60,12 a |
Líquido |
50,00 |
45,83 |
58,33 |
75,00 |
58,33 |
62,50 |
83,33 |
61,90 a |
Médias |
54,16 A |
52,98 A |
58,33 A |
62, 50 A |
62, 50 A |
66,67 A |
70,83 A |
61,01 |
CLONE B |
||||||||
Pó |
79,17 |
91,67 |
87,50 |
83,33 |
95,83 |
83,33 |
87,50 |
86,90 a |
Líquido |
70,83 |
79,17 |
91,67 |
91,67 |
91,67 |
66,67 |
91,67 |
83,33 a |
Médias |
75,00 A |
85,42 A |
89, 58 A |
87,50 A |
93,75 A |
75,00 A |
89,53 A |
85,12 |
CLONE C |
||||||||
Pó |
58,33 |
58,33 |
62,50 |
62,50 |
75,00 |
45,83 |
79,17 |
63,09 a |
Líquido |
25,00 |
75,00 |
70,83 |
25,00 |
75,00 |
50,00 |
79,17 |
57,14 a |
Médias |
41,67 B |
66,67 A |
66,67 A |
43,75 B |
75,00 A |
47,92 B |
79,17 A |
60,12 |
1Médias seguidas pela mesma letra minúscula na coluna e maiúscula na linha não diferem estatisticamente pelo teste de Scott - Knott a 5% e 1% de probabilidade.
Em relação ao número de raízes por miniestaca (NR) (Tabela 5), a diferença entre as concentrações foi significativa de forma que a concentração de 6000mg L-1 de AIB foi melhor para os clones A e B (14,93 e 14,57 raízes/miniestaca, respectivamente) em relação ao tratamento sem aplicação de hormônio (2,34 e 3,59 raízes/miniestaca), e para o clone C não houve diferença, com número de raízes variando de 3,85 a 8,08 raízes/miniestaca independente da concentração de hormônio. Para o clone B, houve diferença significativa entre as formas de aplicação de AIB, em que a aplicação em pó (10,28 raízes/miniestaca) teve melhor resultado que em líquido (8,74 raízes/miniestaca). Na propagação vegetativa, o número de raízes formadas nas estacas é uma das variáveis mais relevantes na produção de mudas além da porcentagem de enraizamento, (Antunes et al., 1996).
TABELA 5- NÚMERO DE RAÍZES POR MINIESTACA DE A. mearnsii DE WILDEMAN APÓS 45 DIAS DE ESTAQUEAMENTO, EM FUNÇÃO DE DIFERENTES CONCENTRAÇÕES DE AIB E DIFERENTES FORMAS DE APLICAÇÃO PARA TRÊS DIFERENTES CLONES A, B E C.
Aplicação de AIB |
Número de raízes por miniestaca |
|||||||
0 mg L-¹ |
1000 mg L-¹ |
2000 mg L-¹ |
3000 mg L-¹ |
4000 mg L-¹ |
5000 mg L-¹ |
6000 mg L-¹ |
Médias |
|
CLONE A |
||||||||
Pó |
2,30 |
6,00 |
7,90 |
8,00 |
10,90 |
10,60 |
15,80 |
8,77 a |
Líquido |
2,40 |
3,60 |
5,70 |
6,70 |
10,90 |
12,30 |
14,10 |
7,95 a |
Médias |
2,34 D |
4,79 D |
6,79 C |
7,33 C |
10,87 B |
11,44 B |
14,93 A |
8,36 |
CLONE B |
||||||||
Pó |
3,70 |
5,50 |
10,50 |
13,40 |
13,10 |
11,50 |
14,30 |
10,28 a |
Líquido |
3,50 |
3,80 |
6,30 |
9,20 |
12,20 |
11,20 |
14,90 |
8,74 b |
Médias |
3,59 D |
4,65 D |
8,44 C |
11,29 B |
12,65 B |
11,37 B |
14, 57 A |
9,51 |
CLONE C |
||||||||
Pó |
3,00 |
7,20 |
5,10 |
6,70 |
5,20 |
4,60 |
8,40 |
5,74 a |
Líquido |
5,90 |
6,00 |
3,40 |
6,80 |
6,70 |
3,10 |
7,80 |
5,66 a |
Médias |
4,44 A |
6,58 A |
4,24 A |
6,71 A |
5,96 A |
3,85 A |
8,08 A |
5,69 |
1Médias seguidas pela mesma letra minúscula na coluna e maiúscula na linha não diferem estatisticamente pelo teste de Scott - Knott a 5% e 1% de probabilidade.
Para a variável comprimento médio de raízes por miniestaca (CMR), na Tabela 6, os valores variaram de 8,62cm, 10,17cm e 8,89cm, respectivamente, entre os clones A, B e C, havendo diferença estatística na concentração de AIB apenas no clone C, com maiores raízes na concentração de 5000mg L-1 de AIB (10,42cm) comparado com miniestacas sem aplicação do hormônio (7,40cm). Para esta característica, o fator que mais diferenciou foi a forma de aplicação de AIB, em que a forma líquida foi mais eficiente para o clone B (10,53cm) e a forma em pó foi mais eficiente para o clone C (9,85cm).
TABELA 6- COMPRIMENTO MÉDIO DE RAÍZES POR MINIESTACA DE A. mearnsii DE WILDEMAN APÓS 45 DIAS DE ESTAQUEAMENTO, EM FUNÇÃO DE DIFERENTES CONCENTRAÇÕES DE AIB E DIFERENTES FORMAS DE APLICAÇÃO PARA TRÊS DIFERENTES CLONES A, B E C.
Aplicação de AIB |
Comprimento médio de raízes por miniestaca (cm) |
|||||||
0 mg L-¹ |
1000 mg L-¹ |
2000 mg L-¹ |
3000 mg L-¹ |
4000 mg L-¹ |
5000 mg L-¹ |
6000 mg L-¹ |
Médias |
|
CLONE A |
||||||||
Pó |
6,50 |
10,10 |
9,50 |
6,80 |
8,20 |
9,30 |
8,80 |
8,45 a |
Líquido |
7,80 |
8,10 |
9,50 |
9,30 |
8,10 |
9,30 |
9,40 |
8,79 a |
Médias |
7,18 A |
9,14 A |
9,46 A |
8,01 A |
8,15 A |
9,31 A |
9,09 A |
8,62 |
CLONE B |
||||||||
Pó |
9,80 |
9,70 |
9,60 |
9,70 |
9,10 |
10,60 |
10,30 |
9,82 b |
Líquido |
10,90 |
10,10 |
10,70 |
10,40 |
11,00 |
10,10 |
10,40 |
10,53 a |
Médias |
10,35 A |
9,90 A |
10,18 A |
10,07 A |
10,03 A |
10,37 A |
10,31 A |
10,17 |
CLONE C |
||||||||
Pó |
10,30 |
9,60 |
8,90 |
9,30 |
9,80 |
10,10 |
11,00 |
9,85 a |
Líquido |
4,50 |
6,60 |
8,50 |
6,20 |
10,10 |
10,70 |
8,90 |
7,93 b |
Médias |
7,40 B |
8,10 AB |
8,67 AB |
7,71 AB |
9,96 AB |
10,42 A |
9,96 AB |
8,89 |
1Médias seguidas pela mesma letra minúscula na coluna e maiúscula na linha não diferem estatisticamente pelo teste de Scott - Knott a 5% e 1% de probabilidade.
Com o aumento da concentração do hormônio AIB, aumenta proporcionalmente a porcentagem de miniestacas enraizadas, o número de raízes/miniestaca e, de forma mais amena, o comprimento médio de raízes por miniestaca (Figura 1). Em todos os casos o clone B apresentou melhor desempenho para o enraizamento, seguido do clone A e o clone C. As análises mostram que os resultados deste trabalho também estão ligados ao genótipo por apresentar diferenças entre os clones abordados, e existe a hipótese de que praticamente todas as espécies de clima subtropical, as quais são tolerantes ao frio, são consideradas recalcitrantes ao enraizamento, o que dificulta em certo ponto estabelecer um protocolo de propagação dessas fontes genéticas em programas clonais (Assis e Mafia, 2007).
Os baixos valores de coeficiente de determinação (R²) para os clones B e C são justificados pelas concentrações de 3000mg L-1 e 5000mg L-1, causando grande variação nos resultados e diminuindo a tendência da reta, mostrando que estas duas concentrações tem pouca influência nos resultados, principalmente, na porcentagem de enraizamento das miniestacas. A capacidade do propágulo em emitir raízes é característica da interação de fatores que se encontram presentes nas células do tecido vegetal e ao estímulo externo, dessa forma, são diversos os fatores que podem afetar significativamente o estado fisiológico da planta-matriz causando alterações no balanço entre promotores e inibidores do enraizamento (HARTMANN et al., 2011), fato este que pode explicar as diferenças nas concentrações de 3000mg L-1 e 5000mg L-1.
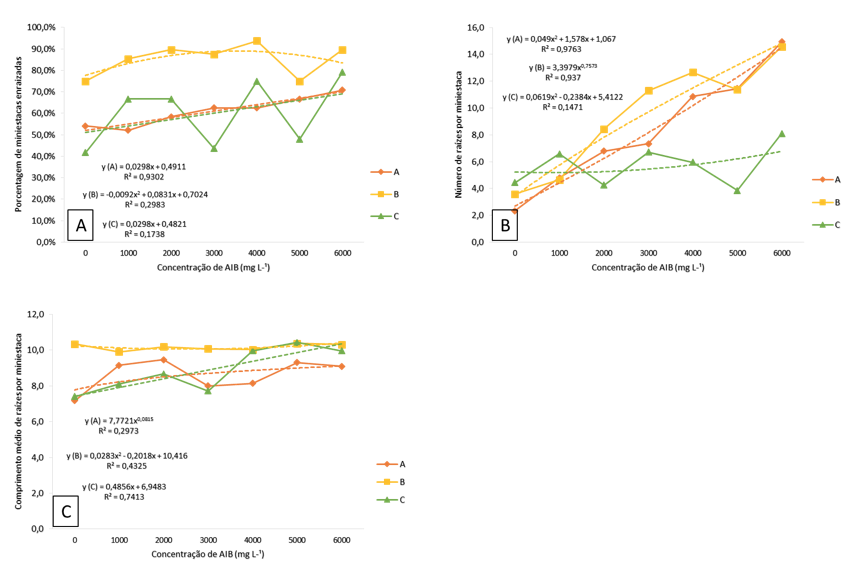
FIGURA 1- ENRAIZAMENTO DE MINIESTACAS DE DIFERENTES CLONES (A,B E C) DE A. mearnsii DE WILDEMAN SOB DIFERENTES CONCENTRAÇÕES DE AIB (0, 1000, 2000, 3000, 4000, 5000 E 6000 MG L-1). A) PORCENTAGEM DE MINIESTACAS ENRAIZADAS; B) NÚMERO DE RAÍZES POR MINIESTACA E C) COMPRIMENTO MÉDIO DE RAÍZES POR MINIESTACA.
Existe predisposição da espécie para o enraizamento, mostrando alta capacidade de formar sistema radicial adventício de qualidade nas condições em que o experimento foi realizado.
A concentração de AIB influencia nas respostas ao enraizamento, bem como na qualidade do sistema radicial, principalmente nas doses de 4000 e 6000mg L-1. Enquanto que a forma de aplicação do regulador tem pouca influência.
O material genético responde de maneira diferenciada ao enraizamento, em que o clone B atinge maiores porcentagens.
À empresa TANAC S.A., pela oportunidade de realização deste trabalho, pela disponibilização do material genético (clones), e pelo apoio financeiro, de pessoal e de infraestrutura.
Alfenas, A.C., Zauza, E. A. V., Mafia, R. G. e Assis, T. F. de. (2004). Clonagem e Doenças do Eucalipto. Viçosa: Universidade Federal de Viçosa.
Almeida, F. D. de, Xavier, A., Dias, J. M. M. e Paiva, H. N. de. (2007). Eficiência das auxinas (AIB e ANA) no enraizamento de miniestacas de clones de Eucalyptus cloeziana F. Muell. Revista Árvore, 31(3), 455-463.
Antunes, L. E. C., Hoffmann, A., Ramos, J. D., Chalfun, N. N. J. e Oliveira Júnior, A. F. de. (1996). Efeito do método de aplicação e de concentrações do ácido indol butírico no enraizamento de estacas semilenhosas de Pyrus calleryana. Revista Brasileira de Fruticultura, 18 (3), 371-376.
Araújo, J. M. A. (1985). Química de alimentos: teoria e prática. Viçosa: Universidade Federal de Viçosa, 1985.
Assis, T. F. e Mafia, R. G. (2007). Hibridação e clonagem. In A. Borém (ed.), Biotecnologia Florestal (pp.93-121). Viçosa: Suprema.
Borges, S. R., Xavier, A., Oliveira, L. S. de, Melo, L. A. de e Rosado, A. M. (2011). Enraizamento de clones híbridos de clones de Eucalyptus globulus. Revista Árvore, 35 (3), 425-434.
Brondani, G. E., Wendling, I., Grossi, F., Dutra, L. F. e Araujo, M. A. (2010). Miniestaquia de Eucalyptus benthamii × Eucalyptus dunnii: (II) sobrevivência e enraizamento de miniestacas em função das coletas e estações do ano. Ciência Florestal, 20 (3), 453-465.
Camargo, P. R. D. e Vieira, E. L. (2001). Aplicações de reguladores vegetais na agricultura tropical. Guaíba: Agropecuária.
Cunha, A. C. M. C. M. da, Wendling, I. e Souza Júnior, L. (2008). Miniestaquia em sistema de hidroponia e em tubetes de corticeira-do-mato. Ciência Florestal, 18 (1), 85-92.
Debergh, P. C. e Read, P. E. (1991). Micropropagation. In P. C. Debergh e R. H. Zimmerman (eds.), Micropropagation technology and application (pp. 486-510). Dordrecht: Kluwer Academic Publishes.
Dias, P. C., Xavier, A., Oliveira, L. S. de, Paiva, H. N. de e Correia, A. C. G. (2012). Propagação vegetativa de progênies de meios-irmãos de angico vermelho (Anadenathera macrocarpa (Benth) Brenan) por miniestaquia. Revista Árvore, 36 (3), 389-399.
Eldridge, K. et al. (1994). Mass vegetative propagation. In K. Eldridge, et al. Eucalyptus domestication and breeding. Oxford: Clarendon Press.
Goulart, P. B., Xavier, A. e Cardoso, N. Z. (2008). Efeito dos reguladores de crescimento AIB e ANA no enraizamento de miniestacas de clones de Eucalyptus grandis x Eucalyptus urophylla. Revista Árvore, 32 (6), 1051-1058.
Haissig, B. E. (1974). Influences of auxins synergists on adventitious root primordium initiation and development. New Zealand Journal of Forestry Science, 4, 311-323.
Hartmann, H. T., Kester, D. E., Davis Jr., F. T. et al. (2011). Plant propagation: principles e practices. Boston: Prentice Hall.
Oliveira, M. C., Ribeiro, J. F., Rios, M. N. da S. e Rezende, M. E. (2001). Enraizamento de estacas para produção de mudas de espécies nativas de matas de galeria. Recomendação Técnica 41. Brasília: Embrapa.
Ono, E. e Rodrigues, J. D. (1996). Aspectos da fisiologia do enraizamento de estacas caulinares. Jaboticabal: FUNEP.
Lattuada, D. S., Spier, M. e Souza, P. V. D. (2011). Pré-tratamento com água e doses de ácido indolbutírico para estaquia herbácea de pitangueiras.Ciência Rural, 41 (12), 2073-2079.
Pallant, J. F. (2005). SPSS survival manual: a step by step guide to data analysis using SPSS. Austrália: Allen & Unwin.
Rêgo, G. M., Zuffellato-Ribas, K. C. e Silva, C. A. de. (2003). Enraizamento de estacas caulinares da corticeira-do-mato (Erythrina falcata (Benth) – Fabaceae). In Congresso Brasileiro de Sementes, 13., Anais... Gramado: ABRATES.
Reis, J. M. R., Chalfun, N. N. J., Lima, L. C. O. e Lima, L. C. (2000). Efeito do estiolamento e do ácido indol butírico no enraizamento de estacas do portaenxerto Pyrus calleryana Dcne. Ciência e Agrotecnologia, 24 (4), 931-938.
Resende, M. D. V. de. (2007). Matemática e estatística na análise de experimentos e no melhoramento genético. Embrapa Florestas: Colombo.
Rezende, A. A. (2007). Enraizamanto de estacas de candeia (Eremanthus Erythrop (DC.)MacLeish). (Mestrado em Florestas de Produção). Universidade Federal de Lavras. Lavras.
Schwarzs, J. L., Glocke, P. L. e Sedgley, M. (2016). Adventitious root formation in Acacia baileyana F. Muell. The Journal of Horticultural Science and Biotechnology, 74 (5), 561-565.
Taiz, L., Zeiger, E. (2004). Fisiologia vegetal. Porto Alegre: Artmed.
Teixeira, J. B. (2001). Limitações ao processo de cultivo in vitro de espécies lenhosas. Brasília: Embrapa-Recursos Genéticos e Biotecnologia.
Titon, M., Xavier, A., Otoni, W. C. e Reis, G. G. dos. (2003). Efeito do AIB no enraizamento de miniestacas e microestacas de clones de Eucalyptus grandis W. Hill ex Maiden. Revista Árvore, 27 (1), 1-7.
Valeri, S. V., Sá, A. F. L., Martins, A. B. G. e Barbosa, J. C. (2012). Enraizamento de estacas de Caesalpinia echinata Lam. em hidroponia. Ciência Florestal, 22 (2), 241-250.
Wendling, I., Ferrari, M. P. e Grossi, F. (2002). Curso intensivo de viveiros e produção de mudas. Documentos 79. Colombo: Embrapa Florestas.
Wendling, I. e Xavier, A. (2005). Influência do ácido indol butírico e da estaquia seria no enraizamento e vigor de estacas de clones de Eucalyptus grandis. Revista Árvore, 29 (6), 921-930.
Xavier, A., Wendling, I. e Silva, R. L. da. (2013). Silvicultura clonal: princípios e técnicas. Viçosa: Universidade Federal de Viçosa.
1. Email: maraluana_pzo@hotmail.com